Anahtar fark: Atomlar, tüm maddelerin yapıldığı temel birimlerdir. Atomlar küçük, genişliği 0.1 ila 0.5 nanometre arasında değişiyor. Herhangi bir elementin her atomu protonlardan, nötronlardan ve elektronlardan oluşur. Moleküler yapmak için farklı elementlerin atomları bir araya gelir. Bu kimyasal bir reaksiyonla olur. Bir molekül, var olabilecek en küçük kimyasal madde miktarıdır.
Bir element atom numarası ile ayırt edilen bir veya bir atom tipine sahip saf bir kimyasal maddedir. Atom numarası, elementin çekirdeğinde bulunan proton sayısından elde edilir. Metal, metaloidler ve metal olmayanlar arasında bölünmüş toplam 118 element vardır. Her eleman kendi özelliklerine sahiptir. Çoğu element dünya üzerinde bulunurken, birkaçı nükleer reaksiyonlarla yapay olarak geliştirilmiştir. Bir eleman zaten rawest şeklindedir ve daha fazla parçalanamaz. Elementlerin tamamı, atom numarası ile listelenen Periyodik Tabloda bulunabilir.
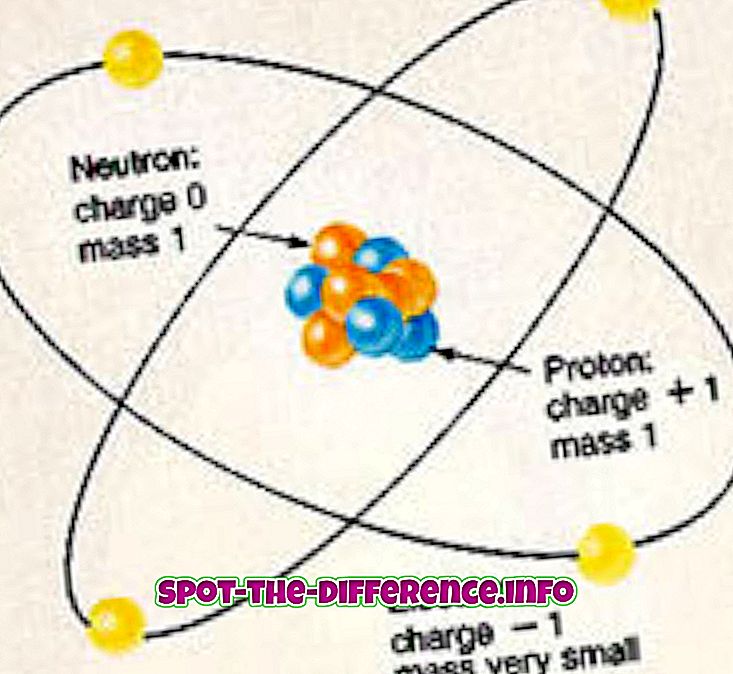
Herhangi bir elementin her atomu protonlardan, nötronlardan ve elektronlardan oluşur. Protonlar ve nötronlar atomun çekirdeğini oluşturur ve atomun ortasında bulunur. Çekirdek, elektromanyetik bir kuvvetle çekirdeğe bağlanan bir elektron bulutu ile çevrilidir. Elektronlar, çekirdekteki protonlar pozitif bir yüke sahip olduklarından çekirdeğe nasıl çekildikleri negatif bir yüke sahiptir. Öte yandan nötronların bir yükü yoktur.
Bir atomdaki proton, nötron ve elektron sayısı hangi element olduğunu belirler. Örneğin: Bir demir atomunun 26 protonu, 30 nötronu ve 26 elektronu vardır. Her demir atomu bu konfigürasyona sahip olacaktır.
Moleküler yapmak için farklı elementlerin atomları bir araya gelir. Bu kimyasal bir reaksiyonla olur. Örneğin: iki hidrojen atomu ve bir oksijen atomu bir su molekülü oluşturmak için birleşir.

Bir molekül, yapıldığı elementlerden çok farklı özelliklere sahip olabilir. Örneğin: su, iki hidrojen atomundan ve bir oksijen atomundan oluşmasına rağmen, oksijen veya hidrojenden çok farklı davranır.
Ayrıca, bir doğaya bir şeye bağlanmadan bağımsız olarak var olamaz. Asla sadece tek bir oksijen atomu veya tek bir karbon atomu bulamayacağız. Her zaman O2 (oksijen) veya CO2 (karbon dioksit) gibi bir şeyle bağlanır. Bir moleküle bağlandığında, molekül doğada bağımsız olarak bulunabilir, bu yüzden her zaman bir oksijen molekülü, bir karbon dioksit molekülü, bir su molekülü (H20), vb. Bulabiliriz.
Bir molekülde, atomlar belirli bir biçimde veya biçimde birbirine yapışır. Bu, temel olarak atomun yapabileceği bağların sayısına bağlıdır. Atomlar birbirleriyle kimyasal bağlar oluşturarak moleküller oluşturur. Oksijen atomları her zaman diğer atomlarla iki bağa sahiptir, karbon atomları her zaman diğer atomlarla dört bağa sahiptir ve azot atomları her zaman diğer atomlarla üç bağa sahiptir. Bundan dolayı, belirli bir molekül tipi her zaman beşgen, altıgen, yanal, iki yanal, vb. Gibi özel bir şekle sahiptir.
Moleküller her zaman birlikte gruplanma eğilimindedir, durumlarına bağlı olarak oluşumları. Gaz halindeki gibi, moleküller sadece uçuşma eğilimindedir. Sıvı halde moleküller, serbestçe hareket edebilmeleri için gevşek bir şekilde gruplanma eğilimindedir. Halbuki katı halde moleküller birbirine sıkıca sarılır ve sadece titreyebilir.
Moleküller genellikle moleküler bir formülde temsil edilir. Örneğin: 02, H20, CO2, C6H12O6 (şeker). Moleküler formül, elemanın adı ve onu izleyen molekül içindeki atom sayısıdır.