Temel Fark: Sıvı, sabit bir şekli olmayan ancak belirli bir hacmi olan bir madde halidir. Sulu bir çözelti, bir maddenin suda çözüldüğü bir çözeltidir.
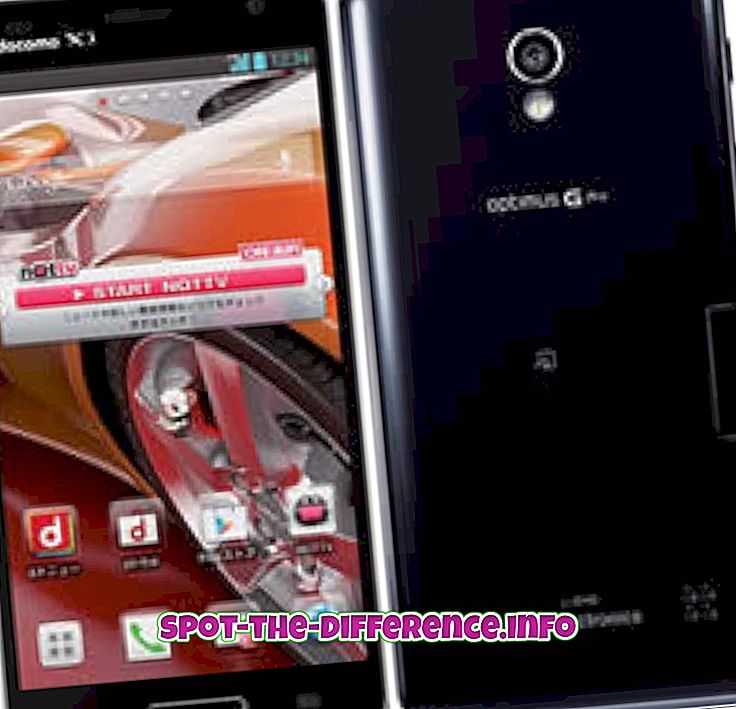
Katı, sıvı ve gaz, nesnelerin Dünya üzerinde bulunabileceği üç ana maddedir. Neredeyse tüm maddeler bu üç durumdan birinde bulunabilir. Su, her üç durumda, buz (katı), su (sıvı) ve buharda (gaz) bulunduğu gibi, maddenin hallerini tanımlamak için kullanılabilecek en iyi örnektir. Sulu, bilimde kullanılan ve suda çözünen bir maddeyi ifade eden bir terimdir. Sıvı ve sulu her ikisi de halde halde olmasına rağmen, birbirlerinden tamamen farklıdır ve birbirlerinin yerine kullanılmamalıdırlar.

Sıvı parçacıklar sıkıca tutturulur, ancak sert bir şekilde bağlanmaz, bu da akma kabiliyeti verir. Ayrıca, sınırlı parçacık hareketliliğiyle, birbirlerine serbestçe hareket edebiliyorlar. Sıvının diğer hallere dönüşümü molekülleriyle ilgilidir; Sıvı ısıtıldığında moleküller, titreşimlerde ve hareketlerde artar ve aralarında daha büyük mesafeler oluşmasına neden olur. Katılaşma sırasında, sıvı soğutuldukça, moleküller bir araya gelir ve kristalleşme olarak bilinen özel bir düzen oluşturur. Aralarındaki bağlar daha sert ve güçlü hale gelir. Su, dünyadaki en bol sıvıdır ve yaşamın devamı için bir zorunluluk olarak kabul edilir.

Hidrofobik bir madde (sudan korkan), suda çözünmeyen bir madde iken, hidrofilik bir madde (su seven) suda çözünen bir maddedir. Tanımlarına göre asitler ve bazlar sulu çözeltilerdir. Bir maddenin suda çözülme kabiliyeti, maddenin su molekülleri tarafından oluşturulan güçlü çekici kuvvetleri aşması veya eşleşmesi ile belirlenir. Madde suyu çözmez ise, bir çökelti oluşturur. Güçlü elektrolit içeren sulu çözeltiler elektrik iletebilir ve verimli iletkenlerdir; zayıf elektrolit içeren çözeltiler ise zayıf elektrik iletkenleridir. İyi iletken maddeler su içinde tamamen iyonize olurken zayıf iletkenler sadece küçük bir iyonlaşma derecesine sahiptir. Sulu çözelti örnekleri arasında ev tipi ağartma maddesi, kan, boya ve süt bulunur.