Anahtar Fark: Difüzyon, moleküllerin toplu hareket gerektirmeden bir yerden bir yere hareket ettiği ve hareket ettiği süreçtir. Efüzyon, moleküllerin bir iğne deliğinden geçerek yüksek konsantrasyonlu bir yerden düşük konsantrasyona kadar olan süreçtir.
Difüzyon ve efüzyon terimleri genellikle kimya, fizik ve biyoloji gibi birçok bilimlerde kullanılmaktadır. Kimyada bu iki terim gazların iki özelliğidir. Bu ikisi, yalnızca gazların temelini ve özelliklerini öğrenen birçok insan için kafa karıştırıcı. Difüzyon ve Efüzyon, iki farklı anlam ifade eden ve birbirinin yerine kullanılmaması gereken iki farklı terimdir. Difüzyon, gazların birbiriyle karışabilme kabiliyetini belirtirken, efüzyon gazın küçük bir pim deliğinden geçmesini sağlar. Yayılma aynı zamanda sosyoloji, ekonomi ve finansta da insanların, fikirlerin ve değerlerin yayılmasını ifade etmek için kullanılır.
Difüzyon, moleküllerin kütle hareketi gerektirmeden bir yerden bir yere hareket ettiği ve hareket ettiği süreçtir. Difüzyon, moleküllerin sadece kinetik enerji kullanarak hareket etmesi veya karışması ile sonuçlanır. "Difüzyon" kelimesi, "yayılmak" anlamına gelen "diffundere" Latince kelimesinden türemiştir. Difüzyonda, moleküller sabit bir hareket halindedir ve kinetik veya termal enerji ile tahrik edildiğinde ayrılmaz bir karışım ile sonuçlanan diğer moleküller ile karışmaya meyillidirler. Pratik bir yaklaşım alalım, bir kap katı bölüm kullanarak A & B bölümlerine ayrılmıştır; ilk bölüm su ile doldurulurken, ikinci bölüm kırmızı boya ile doldurulur. Şimdi, bölme kaldırıldığında, boya ve su tüm kabı doldurmaya çalışmaktadır. Ardından boya yavaşça suya kırmızıyla temas eder, bu difüzyondur.
Difüzyon, moleküllerin daha yüksek konsantrasyon alanlarından daha düşük konsantrasyon alanlarına kaymalarına neden olarak tüm moleküllerin karışımına neden olur. Tüm moleküller eşit bir şekilde yayıldığında difüzyon durur. Difüzyon su ile sınırlı değildir ve moleküllerin daha fazla enerjiye ve diğer moleküllerle karışma kabiliyetine sahip olduğu gaz hallerinde en iyi şekilde çalışır. Difüzyona iki yaklaşım vardır: fenomenolojik ve atomistik. Fenomenolojik yaklaşıma göre moleküller, yüksek konsantrasyonlu bölgelerden düşük konsantrasyonlu bölgelere hareket eder. Atomistik yaklaşımda, difüzyonun birlikte karışmasına neden olan termal enerji tarafından itildiği difüzyon parçacıklarının rastgele yürüyüşü nedeniyle difüzyonun gerçekleştiği düşünülmektedir. Difüzyon, vücudun ihtiyaç duyduğu minerallerin, besinlerin ve enerjinin oluşturulmasında önemli bir rol oynar.

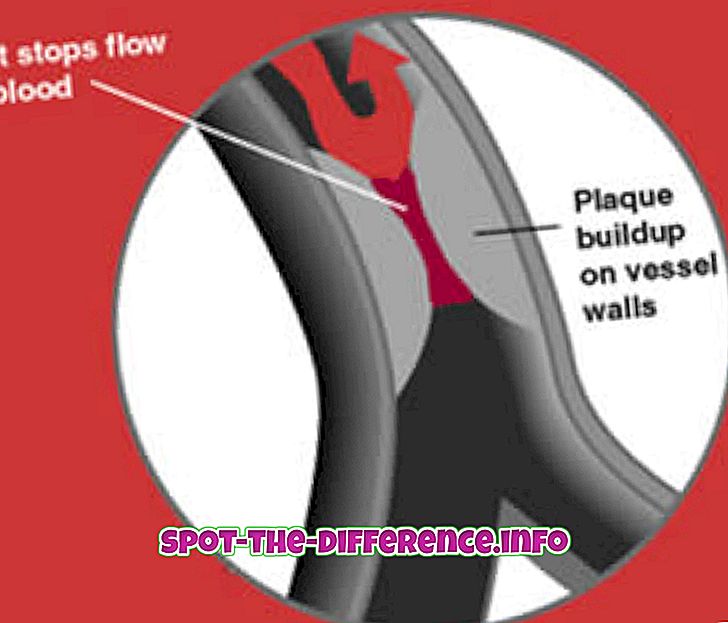
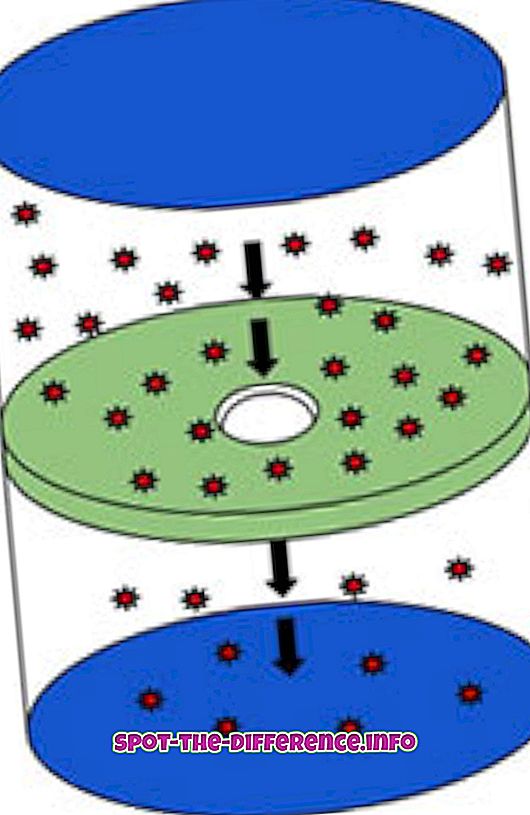
Efüzyon, moleküllerin bir iğne deliğinden geçerek yüksek konsantrasyonlu bir yerden düşük konsantrasyona kadar olan süreçtir. İşlem, gazın moleküller arasında çarpışma olmadan küçük bir delikten geçme kabiliyetini açıklar. Bu, deliğin çapı, moleküllerin ortalama serbest yolundan oldukça küçük olduğunda meydana gelir. Ortalama serbest yol, ardışık çarpışmalar arasında hareketli bir parçacık tarafından kat edilen ortalama mesafedir. Bunun pratik bir örneği, bir kabı bir şişeyle dumanla doldurmak ve şişeye küçük bir delik açmaktır, delikten dışarı fırlamaya başlayan duman efüzyon olarak kabul edilir.
Efüzyon ölçümü için formülü oluşturan İskoç kimyager Thomas Graham, gazın ne kadar hızlı hareket edeceğini ve nasıl ölçülebileceğini belirleyen bir Graham Yasası yarattı. Graham Yasasına göre, gazların tükenme hızı moleküler ağırlıklarına bağlıdır. Daha düşük moleküler ağırlığa sahip gaz, daha yüksek moleküler ağırlığa sahip bir gazdan daha hızlı bir şekilde akacaktır. Efüzyon, bir saniyede delikten kaç molekülün geçtiğini ölçerek hesaplanır. Benzer şekilde, termodinamikte bir gazın efüzyon hızı, parçacıklarının kütlesinin kare kökü ile ters orantılıdır.