Temel Fark: Molarite, molar konsantrasyon olarak da bilinir, bir litre çözelti başına mevcut bir maddenin mol sayısını ölçer. Molarite, büyük M harfi ile gösterilir. Molality, bir kilogram çözücü için mevcut bir maddenin mol sayısını ölçer. Molalite küçük harf m ile gösterilir.
Her iki kavram da hesaplamalarını mevcut çözümde kaç mol bulunduğuna dayandırıyor. Bir çözelti, homojen bir karışım olarak tanımlanabilir; bu, iki veya daha fazla bileşenin çıplak gözle ayırt edilemeyeceği noktaya kadar karıştırıldığı anlamına gelir. Bu iki kavram, çözeltide mevcut olan mol sayısını belirlediği için molleri anlama gerektirir. Mol teorisi İtalyan bilim adamı Amedeo Avogardo tarafından keşfedildi.
1811'de Avogardo, belirli bir sıcaklık ve basınçtaki gaz hacminin, doğasından bağımsız olarak atom veya molekül sayısı ile orantılı olduğunu öne sürdü. Bu kavram Avogardo sabiti olarak bilinir. Belirli bir maddenin bir molündeki bileşen partiküllerin sayısı (genellikle atomlar veya moleküller) olarak tanımlanır. Laymen cinsinden, bir maddenin bir molü elementte mevcut olan atom ve molekül sayısını temsil edecektir. Örneğin: Oksijen 16'lık bir atom ağırlığına sahiptir, bu oksijen molü başına kütleyi temsil eder. Böylece, bir mol oksijen 16 gramlık bir kütleye sahip olacaktır. Avogardo'ya göre, bir mol oksijen, bir mol hidrojen ile aynı sayıda atoma sahip olacaktır. Bununla birlikte, ağırlık olarak farklılık gösterebilirler.
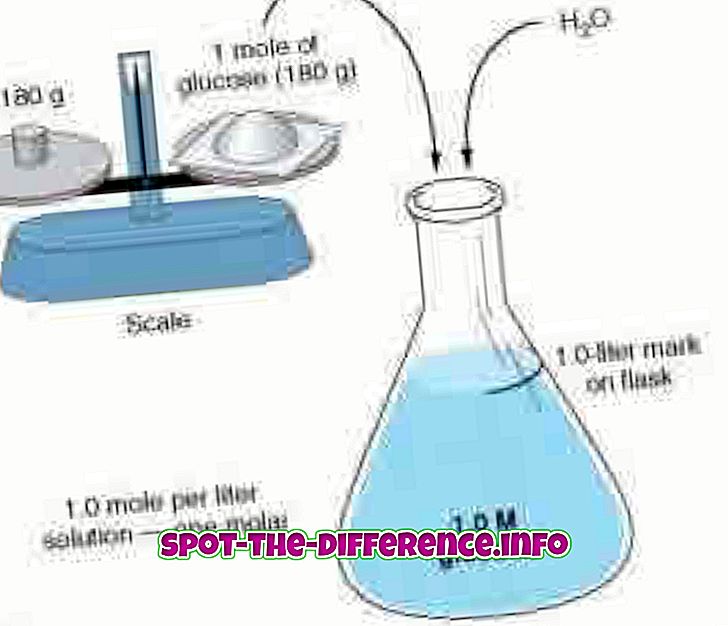
Molarite ve molalite iki farklı yaklaşım kullanarak konsantrasyonu ölçer. Molarite, molar konsantrasyon olarak da bilinir, bir litre çözelti başına mevcut olan bir maddenin mol sayısını ölçer. Molarite, büyük M harfiyle ifade edilir. Dolayısıyla, 1.0M olan bir çözelti, bir litre çözelti başına 1 mol çözünen içerdiğini belirtir. Örneğin: Bir su ve şeker çözeltisi. Çözelti 1, 0 M olarak ölçülürse, çözelti mevcut çözelti litre başına 1 mol şeker içerir. Molarite ayrıca, madde miktarı konsantrasyonu, miktar konsantrasyonu, madde konsantrasyonu veya basitçe konsantrasyon olarak da bilinir. Molarite, aşağıdaki formül kullanılarak hesaplanabilir: M = mol (mol sayısı) / L (litre cinsinden çözelti hacmi).

Molalite, bir kilogram çözücü için mevcut bir maddenin mol sayısını ölçer. Molalite küçük harf m ile gösterilir. Dolayısıyla, 1.0m olan bir çözelti, bir kilogram çözücü için 1 mol çözünen içerdiğini belirtir. Çözücüden çözüneni ayırt edelim. Çözünme, başka bir maddeye çözülen maddedir. Bir çözücü, çözüneni çözen bir maddedir. Bu nedenle, eğer su ve şeker bir arada karıştırılıyorsa, şeker çözünen olur ve çözücü sulanır. Karışık şeker suyu çözelti olacaktır. Şimdi, molalitede, mollerin çözelti değil çözücünün kütlesiyle bölünmesi büyük önem taşımaktadır. Molalite, aşağıdaki formül kullanılarak hesaplanabilir: m = mol (mol sayısı) / KG (kg cinsinden çözücü kütlesi).
Neden fark? Her ikisi de sıcaklıkla uğraşırken kullanılır. Eğer bir çözelti sıcaklıkta değişecekse, molalite kullanılır. Fakat sabit sıcaklıkta kalacak çözeltiler için molarite kullanılır. Bunun nedeni sıcaklık yükselip alçaldıkça çözeltinin hacminin değişmesi ve bunun molariteyi doğrudan etkilemesidir. Dolayısıyla, molalite konsantrasyon hesaplamak için kullanılır.